Апластическая анемия: симптомы и лечение
Оглавление: 1. Апластисческая анемия: что это такое 2. Причины апластической анемии 3. Патогенез 4. Классификация 5. Симптомы апластической анемии 6. Осложнения 7. Диагностика апластической анемии, анализ крови 8. Лечение апластической анемии 9. Профилактика и прогноз
Апластисческая анемия: что это такое
Апластическая анемия – гематологический синдром, отражающий угнетение эритроцитарного, лейкоцитарного и тромбоцитарного ростков костного мозга. Встречаются и изолированные дефициты эритроцитов. Первое описание патологии в 1888 году принадлежит немецкому иммунологу, основателю химиотерапии, Паулю Эрлиху. Заболеваемость в Европе составляет 4-5 случаев на 1000000 человек. Типично заболевают молодые (до 20 лет) и старшие возрастные группы (после 65). Распространенность выше в регионах с химическим производством, агрессивным использованием сельскохозяйственных удобрений. У молодых роль играет вирусная инфекция, запускающая иммунные процессы в организме.
Причины апластической анемии
Четкую зависимость возникновения заболевания от определенного фактора можно проследить не более, чем у половины пациентов. Встречаются как врожденные варианты на фоне наследуемых или спровоцированных хромосомных аномалий, так и приобретенные. Базовая причина — иммунная агрессия против клеток-предшественников кроветворения. Ее провоцируют:
- Физические и химические агенты: ароматические углеводороды, ионизирующее излучение, алкилирующие агенты, антиметаболиты (антиагонисты пурина, фолиевой кислоты).
- Лекарства: хлорамфеникол (левомицетин), нестероидные противовоспалительные (фенилбутазон), препараты золота (натрия ауротиомалат), инсектициды.
- Гепатиты (вирусные, алкогольные, токсические). При этом нет прямой зависимости риска развития аплазии от тяжести воспаления печени. Даже после выздоровления от гепатита может появиться анемия.
- Вирусы: цитомегаловирус, Эпштейн-Барр, гепатитов В, С, Д, Е.
- Беременность снижает иммунную защиту. Даже после рождения плода риски развития костномозговой недостаточности сохраняются.
- Прочие заболевания: пароксизмальная ночная гемоглобинурия, туберкулез, тимома, зоб Хошимото, хронический лимфобластный лейкоз, лимфома.
Если причина точно не установлена, то апластическая анемия считается идиопатической.
Патогенез
Иммунные реакции против ростков кроветворения способны запускать самые разные химические соединения. Важно ограничить бесконтрольное поступление в организм лекарств и бытовых ядохимикатов.
Классификация
Патологию разделяют в зависимости от этиологических факторов на наследственную и приобретенную. Приобретенная может быть идиопатической, лекарственной, токсической, вирусной. Кроме классической панцитогемопении с угнетением всех ростков кроветворения существует и парциальная эритроцитарная гипоплазия, затрагивающая только эритроциты. По степеням тяжести выделяют:
- нетяжелую (снижение числа гранулоцитов > 0,5х109),
- тяжелую (<0,5х109),
- сверхтяжелую (<0,2х109).
Тяжесть болезни определяется результатами трех анализов крови до начала терапии. Об устойчивой форме говорят в случае неэффективности комбинированной иммуносупрессивной терапии на протяжении 6 месяцев. Выделяются варианты течения с присоединением пароксизмальной ночной гемоглобинурии или без нее.
Симптомы апластической анемии
Возможно острое начало или постепенное развитие признаков заболевания. Клиническая картина складывается из анемического, геморрагического, септико-некротического синдромов. Они могут проявиться совокупно или один из них преобладает.
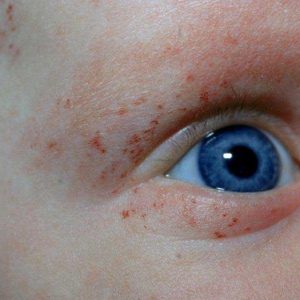
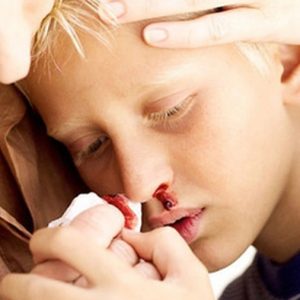
- Нехватка тромбоцитов провоцирует точечные, пятнистые, спонтанно возникающие кровоизлияния в кожу и слизистые. Бывают носовые, маточные (у женщин), желудочные кровотечения. Кровоточат десны. Растут риски гематурии.
- Лейкопения и агранулоцитоз ведут к частым ОРВИ, инфекциям мочевыводящих путей, ЛОР-органов. Типичен фурункулез, бронхиты. Развиваются нетипичные пневмонии (пневмоцистные, микоплазменные), саркомы Капоши. Нередки распространенные формы кандидоза, герпес.
Наследуемая по аутосомно-рецессивному типу апластическая анемия Фанкони обычно дебютирует у детей моложе 10 лет. Помимо анемии, агранулоцитоза и тромбоцитопении отмечается низкий рост, непропорционально маленькая голова. Недоразвитие трубчатых костей конечностей сочетается с аномалиями пальцев рук, врожденным вывихом бедра, деформациями стоп. Патологии зрительного анализатора сводятся к косоглазию, опущениям век, недоразвитию глазных яблок. Могут регистрироваться глухота, умственная отсталость. Типичны недоразвития половой системы, отставание в половом созревании. Они сочетаются с дефектами мочевыводящей системы, кардиальными пороками. Если заболевание развилось в детстве, больные редко доживают до 30 лет. У взрослых анемия данного типа развивается до 40 лет, сочетается с острым миелоидным лейкозом.
Банальная усталость в сочетании с носовыми кровотечениями или кровоточивостью десен может оказаться началом такого грозного состояния, как апластическая анемия.
Осложнения
Регистрируются такие основные последствия заболевания, как геморрагический синдром (гастродуоденальные кровотечения, кровоизлияния во внутренние органы и серозные сумки, мозговой инсульт). Инфекционные осложнения представлены пневмониями, пиелонефритом, провоцируемые вирусными или атипичными бактериальными возбудителями, с тяжелым течением, частой функциональной недостаточностью внутренних органов. Самыми грозными могут считаться инфекционно-токсический шок, сепсис, увеличивающие риски неблагоприятного исхода. Прогрессирующая апластическая анемия может привести к коме.
Осложнения от иммуносупрессивной терапии по своей тяжести сравнимы с вредом основной патологии. Токсичность в отношении ЖКТ, почек, развитие энцефалопатии – лишь малая часть последствий лечения цитостатиками. Медикаментозное подавление иммунитета ведет к вторичным инфекциям грибковой, вирусной природы. Особенно опасно опустошение костного мозга в период перед его пересадкой. Это требует тщательного лабораторного контроля за пациентом и назначения адекватной противоинфекционной терапии. На фоне иммуносупрессоров могут развиваться и аллергические реакции.
Диагностика апластической анемии, анализ крови
Заболевание можно заподозрить по жалобам пациента на слабость, утомляемость, повышенную кровоточивость и частые инфекции кожи, дыхательных и мочевых путей. При осмотре обращают на себя внимание бледность кожи и слизистых, одышка, учащенный пульс, пониженное артериальное давление. Выслушивается тахикардия, систолический функциональный шум в проекции верхушки сердца. Базовые критерии диагностики – лабораторные исследования.
- Клинический анализ крови фиксирует трехростковую цитопению. Гемоглобин < 110 г/л подтверждает анемию. Гранулоциты<2х109 г/л – гранулоцитопению, тромбоцитопению – тромбоциты < 100х109/л. Анемия нормохромная.
- Микроскопия мазка показывает снижение ретикулоцитов, нейтропению с относительным лимфоцитозом. Среди эритроцитов преобладают макроциты.
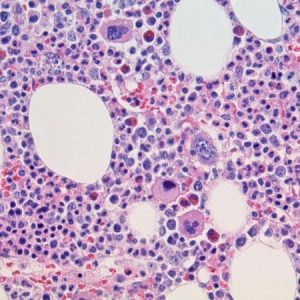
- Исследования костномозговых тканей представлены двумя пробами. Пунктат из грудины обеднен клетками, среди которых полностью отсутствуют мегакариоциты. Материал биопсии подвздошной кости демонстрирует аплазию (замещение ростковых клеток жировыми).
Лечение апластической анемии
Ведением пациентов с момента диагностики занимается врач-гематолог. Программа терапии складывается из нескольких этапов.
- Комбинированная иммуносупрессия. Включает антимоцитарный глобулин, циклоспорин, назначаемые курсами на протяжении года и более. Геморрагический синдром и инфекционные процессы должны быть подавлены еще до начало терапии супрессорами. Возможно одновременное лечение донорским тромбоцитами и циклоспорином. Дополнительно могут использоваться триметоприм и глюкокортикостероиды.
- Стимуляторы или активаторы кроветворения. Основным активатором кроветворения, используемым в терапии данной патологии, становится Элтромбопаг. Препарат симулирует работу собственного тромбопоэтина. Его активация сопровождается запуском дифференцировки мегакариоцитов.
- Заместительные переливания компонентов крови: эритромассы, тромбоконцентрата. Тяжелый геморрагический синдром с жизнеугрожающими кровотечениями требует трансфузий плазмы.
- Препараты, уменьшающие накопление железа в органах и тканях. Показаны при уровне ферритина сыворотки > 1000 нг/мл у пациентов с рефрактерной формой болезни. Основной препарат – Деферазирокс.
Хирургическое лечение показано при непереносимости антимоцитарного глобулина, включает удаление селезенки. Спленэктомия входит и в программу подготовки к миелотрансплантации. Максимально благоприятные отдаленные последствия у аллогенной костномозговой пересадки.
Результаты лечения могут оцениваться, как ремиссия, в случае отсутствия потребности в заместительных гемотрансфузиях, полных или частичных улучшений гемограммы. Гемоглобин должен подняться выше 100 г/л, гранулоциты >1,5х109 г/л, тромбоциты > 100х109 г/л. Оценка терапии проводится через 3 месяца, полгода, год, 18 месяцев и 2 года.
Профилактика и прогноз
Если иммуносупрессивная терапия начата максимально рано, адекватно поддержана заместительными переливаниями компонентов крови и противоинфекционными препаратами, у пациента имеются все шансы на длительную ремиссию. Радикально заболевание возможно вылечить путем аллогенной костномозговой пересадки. Ремиссии в таком случае удается добиться у 90% пациентов.
Профилактические мероприятия для предотвращения наследственных форм патологии сводятся к генетическому обследованию потенциальных родителей еще до зачатия. Риски развития приобретенных форм удается снизить только рациональным приемом лекарств, ограничением интоксикаций, своевременной вакцинацией от вирусных гепатитов, адекватной терапией инфекционных и аутоиммунных заболеваний.
Мария Постнова, терапевт, медицинский обозреватель
4,108 total views, 2 views today


 (64 голос., средний: 4,25 из 5)
(64 голос., средний: 4,25 из 5)